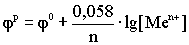К активным
металлам относится те, мера растворимости которых
больше концентрации солевых растворов, принятых в электрохимии.
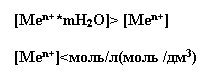
Если металл является
активным, то равновесие обратимой реакции смещено в прямом направлении,
т.е. в сторону окисления:
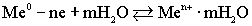
Возникающий электродный потенциал
имеет знак "-".
Пассивные металлы
те, у которых величина растворимости меньше принятой в электрохимии
концентрации солевых растворов.
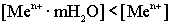
В данном случае равновесие реакции
смещено в обратном направлении, т.е. в сторону восстановления. Возникающий
электрический потенциал имеет знак "+".
Величина
равновесного электродного потенциала
Нернст установил эту величину
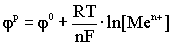 ,
где
,
где
φ0 – стандартный электродный
потенциал, т.е. потенциал, возникающий при нормальных условиях,
R - универсальная газовая постоянная,
Т - абсолютная температура, К,
F - число Фарадея, F = 96500 Кл,
n - число электронов, участвующих в реакции.
Переходя от натурального логарифма
к десятичному и подставляя в уравнение значение T=298K и соответствующие
значения R и F, получаем выражение: