ЛЕКЦИЯ N 8
Уравнение Шредингера для
атома водорода.
Квантовые числа.
Спектры атома водорода в теории Шредингера.
Волновая функция основного состояния атома
водорода
§ 1. Уравнение Шредингера для атома водорода
В лекции N 7 мы разобрали боровскую теорию атома
водорода, основанную на постулатах Бора и условии стационарности
состояний атома (4.3).
Уравнение Шредингера, примененное к атому водорода,
позволяет получить результаты боровской теории атома водорода
без привлечения постулатов Бора и условия квантования. Квантование
энергии возникает как естественное условие, появляющееся при решении
уравнения Шредингера, в некотором смысле аналогичное причине квантования
энергии для частицы в потенциальной яме. Применить стационарное
уравнение Шредингера (7.3) к атому водорода это значит:
а) подставить в это уравнение выражение для
потенциальной энергии взаимодействия электрона с ядром
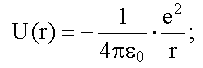
б) в качестве m подставить
me - массу электрона (если
пренебречь, как и в лекции N 4, движением ядра).
После этого получим уравнение
Шредингера для атома водорода:
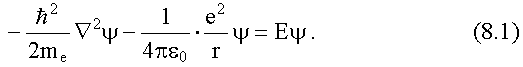
Так как потенциальная энергия зависит только
от r, решение уравнения удобно искать в сферической системе координат:
r, θ, φ.(рис. 8.1)
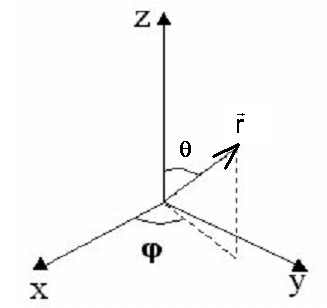
Рис. 8.1
Волновая функция в этом случае будет функцией
от r, θ и φ,
т.е.
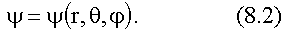
Оператор Лапласа 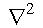 необходимо записать в сферических координатах, т.е. выразить через
производные по r, θ и φ.
Мы не будем этого делать, поскольку получение решения уравнения
Шредингера для атома водорода не входит в программу курса общей
физики. Приведем лишь результаты.
необходимо записать в сферических координатах, т.е. выразить через
производные по r, θ и φ.
Мы не будем этого делать, поскольку получение решения уравнения
Шредингера для атома водорода не входит в программу курса общей
физики. Приведем лишь результаты.
Оказывается, что решение уравнения Шредингера
для атома водорода существует при следующих условиях:
а) при любых положительных значениях полной
энергии (E > 0). Это так называемые
несвязанные состояния электрона, когда он пролетает
мимо ядра и уходит от него на бесконечность;
б) при дискретных отрицательных значениях энергии
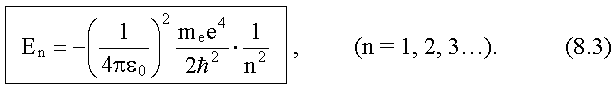
Эта формула совпадает с полученной Бором формулой
для энергии стационарных состояний атома водорода. Целое число
n называют главным
квантовым числом.
§ 2. Квантовые числа
Волновые функции электрона ψnlm(r,
θ, φ) определяются тремя целочисленными параметрами:
n, l, me.
Эти целые числа называются квантовыми
числами:
n - главное квантовое число,
оно, как мы знаем (см. (8.3)), определяет значение энергии En,
n=1,2,3┘;
l
- азимутальное (орбитальное) квантовое число, оно определяет
L - модуль момента импульса электрона.

При заданном n азимутальное
квантовое число l может принимать
следующие значения:

всего n значений.
Следовательно, из уравнения Шредингера вытекает,
что момент импульса электрона в атоме
водорода квантуется и может принимать n значений.
Так при n = 1 азимутальное квантовое число
может принимать единственное значение l = 0.
При n = 2 возможны значения l
= 0,1.
ml -
это магнитное квантовое число.
Из уравнения Шредингера также следует, что проекция
момента импульса L на выбранное направление
в пространстве, скажем, ось z, также квантуется.
Величина этой проекции, Lz, связана
с квантовым числом ml.

При заданном l
магнитное квантовое число ml
может принимать следующие значения:
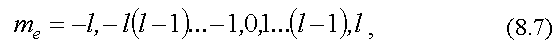
всего 2l + 1 значений.
Значит, при заданной главным квантовым числом
n энергии En
возможны n значений азимутального квантового
числа (от l = 0
до n - 1) и 2l + 1
значений магнитного квантового числа ml..
Таким образом, при заданном n число различных волновых функций
ψnlm, отвечающих заданной
энергии En, будет равно

Говорят, что уровень энергии En
будет вырожден с
кратностью n2.
В атомной физике применяют заимствованные из
спектроскопии условные обозначения состояний электрона с различными
значениями момента импульса:
l
= 0 - s-состояние;
l
= 1 - p-состояние;
l
= 2 - d-состояние;
l
= 3 - f-состояние;
затем идут g, h и дальше
в алфавитном порядке.
Значение главного квантового числа n
указывают перед буквой, являющейся условным обозначением азимутального
квантового числа l.
Например, 1s-состояние
- это состояние с главным квантовым числом n =
1 и азимутальным квантовым числом l =
0 (на это указывает буква s).

