ЛЕКЦИЯ N 9
§ 3. Молекула
Молекула состоит из атомов, связанных друг с другом за счет валентных электронов. Квантовая механика позволяет выяснить физическую природу этой химической связи.
Молекула представляет собой связанную систему ядер и
электронов, между которыми действуют электростатические силы.
Кроме электростатических сил в квантово-механическом рассмотрении
молекулы необходимо учитывать принцип Паули, который приводит
к существованию дополнительного обменного
взаимодействия.
Различают два типа связи в молекулах: ковалентную и полярную.
Ковалентная (гомеополярная)
связь осуществляется за счет обобществления электронов,
принадлежащих двум атомам.
Простейшей молекулой с ковалентной связью является
молекула водорода. В 1927 г. немецкие физики Гайтлер и Лондон
решили уравнение Шредингера для системы, состоящей из двух протонов
(ядра атома водорода) и двух электронов. Оказалось, что энергия
E молекулы водорода по разному зависит от
расстояния r между ядрами для случаев параллельной
и антипараллельной ориентации спинов электронов. График этой зависимости
приведен на рисунке 9.2, из которого видно, что связанное состояние
с E < 0 возможно лишь при антипараллельной
ориентации спинов.
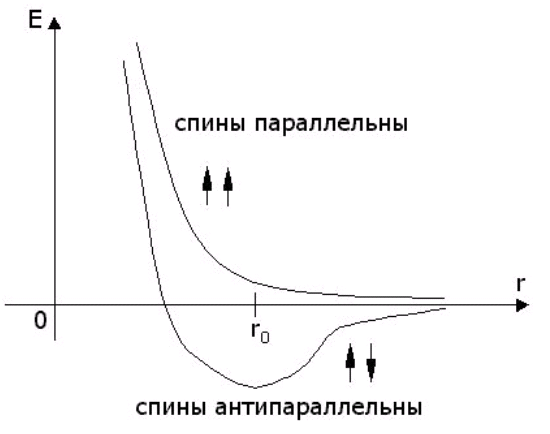
Рис. 9.2
За начало отсчета энергии молекулы E
на графике принята энергия двух изолированных атомов. При r
= r0 график с антипараллельными спинами имеет
минимум, определяющий равновесное положение ядер в молекуле водорода.
Электроны большую часть времени проводят между ядрами, таким образом,
положительные ядра притягиваются к отрицательному "электронному
облаку".
Ионная (гетерополярная) связь
обусловлена переходом валентных электронов с одного атома на другой
с образованием положительных и отрицательных ионов с электростатическим
притяжением между ними.
Характерный пример ионной связи -
NaCl (поваренная соль). Такого типа связь будет и у NaF.
На схеме заполнения электронных состояний, приведенной в §
2 настоящей лекции (рис. 9.1) видно, что у фтора (F)
не заполнено одно квантовое состояние 2p,
а у натрия (Na) один валентный электрон
находится в состоянии 3s, где он сравнительно
слабо связан со своим атомом. Этот 3s электрон
натрия и переходит в 2p состояние атома
фтора. Таким образом, атом Na становится
положительным ионом, а атом F - отрицательным,
поэтому они и притягиваются друг к другу.
Энергия изолированной молекулы
может быть приближенно представлена в следующем виде:
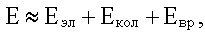
здесь Eэл -
электронная энергия, она обусловлена электронной конфигурацией
в молекуле;
Eкол - энергия
колебания ядер относительно центра масс молекулы;
Eвр - энергия вращения
ядер относительно центра масс молекулы.
Порядки величин Eэл,
Eкол и Eвр
следующие:
Eэл ~ 1 ÷10 эВ;
Eкол ~ 10-2 ÷10-1
эВ;
Eвр ~ 10-5 ÷10-3
эВ.
Каждая из составляющих энергии
Eэл, Eкол и Eвр
квантуется. Ввиду большого различия в их величинах изобразить
энергетическую схему уровней молекулы в масштабе не представляется
возможным. На рисунке 9.3 изображены два электронных уровня Eэл1
и Eэл2 и система колебательных
и вращательных уровней.
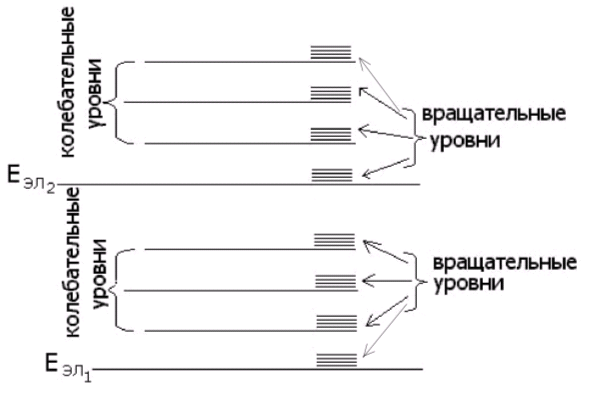
Рис. 9.3
§ 4. Объяснение температурной зависимости теплоемкостей газов
В части 4, лекции N 4 обсуждались графики экспериментальных
зависимостей теплоемкости CV
для двух газов: одноатомного аргона (Ar)
и двухатомного водорода (H2).
Ход графика для аргона соответствовал предсказаниям классической
теории теплоемкости: у одноатомного газа три степени свободы (i
= 3), соответственно CV
= (i/2)R = (3/2)R во всем диапазоне температур. Двухатомный
водород имеет i = 7 (3 поступательные, 2
вращательные, 2 колебательные степени свободы, см., классическая
теория дает для него значение CV = (7/2)R.
Однако, как показывает опыт, водород ведет себя как газ с переменным
числом степеней свободы. Они как бы "вымораживаются": при низких
температурах i = 3, затем при T
> 100K число степеней свободы плавно(!) увеличивается
и достигает 5 при T ≈ 400K. Затем
до T ≈ 800K число степеней свободы
остается постоянным, а дальше опять плавно растет до значения
i = 7.
Такое поведение теплоемкости становится понятным
если учесть квантование вращательного и колебательного движений
молекулы. Поступательное движение не квантуется и его вклад в
теплоемкость (i = 3) присутствует всегда.
При низких температурах, когда средняя энергия теплового движения
молекулы (ε ~ kT) меньше, чем квант
энергии вращательного движения (см. схему уровней в предыдущем
параграфе), тепловое движение не способно возбудить вращение молекулы
и она ведет себя как частица без внутренней структуры с числом
степеней свободы i = 3. Затем, с ростом
T, у наиболее энергичных молекул начинают
возбуждаться вращательные степени свободы, этим объясняется плавный
рост теплоемкости, соответствующий появлению нецелых значений
числа i. Колебательные степени свободы возбуждаются
при более высоких температурах, т.к. расстояние между колебательными
уровнями значительно больше, чем расстояние между вращательными.
Итоги лекции N 9
-
Электрон обладает собственным моментом импульса
LS , не связанным с движением
в пространстве. Модуль собственного момента импульса определяется
спиновым квантовым числом S (см. (9.1)):
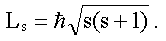
-
Проекция спина на ось z LSz
квантуется (см. (9.2)):
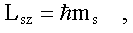
здесь ms - магнитное
спиновое квантовое число, для электрона (см. (9.3)):
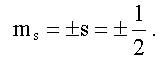
-
Квантовое состояние электрона в любом
атоме задается четырьмя квантовыми числами:
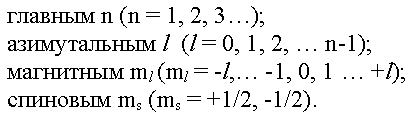
-
Частицы с полуцелым спином s
относятся к фермионам (например - электрон),
а частицы с целым спином - к бозонам (например
- фотон).
-
Принцип Паули утверждает, что в квантовой
системе фермионов две частицы не могут находиться в одном
и том же квантовом состоянии.
-
Бозоны не подчиняются принципу Паули, они
могут находиться в одинаковом квантовом состоянии в неограниченном
количестве.
-
Периодическое повторение химических свойств
элементов с ростом зарядового числа Z,
открытое Д.И. Менделеевым, объясняется заполнением электронами
квантовых состояний в атоме с учетом принципа Паули.
-
В молекулах различают два типа связи: ковалентную
и полярную.
-
Ковалентная связь осуществляется
за счет обобществления электронов, принадлежащих двум атомам.
-
Ионная связь обусловлена переходом электронов
с одного атома на другой с образованием положительных и отрицательных
ионов с электростатическим притягиванием между ними.
-
Энергия изолированной молекулы может быть
приближенно представлена в виде:
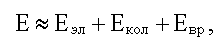
здесь
Eэл - электронная энергия, она
обусловлена электронной конфигурацией в молекуле; Eкол
- энергия колебания ядер относительно центра масс молекулы Eвр
- энергия вращения ядер относительно центра масс молекулы.
Порядки величин Eэл,
Eкол и Eвр
следующие:
Eэл ~ 1 ÷10
эВ;
Eкол ~ 10-2
÷10-1 эВ;
Eвр ~ 10-5
÷10-3 эВ.
-
Квантование колебательной и вращательной
энергии молекулы объясняет экспериментально наблюдаемую зависимость
теплоемкостей газов от температуры (см. § 4).

