Гибридизация электронов
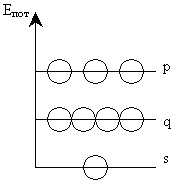
происходит по форме и энергии. S- и р – облака образуют гибридные
q – облака, имеющие конфигурацию
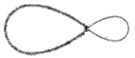 .
.
 |
В атоме
углерода происходит SP3 – гибридизация, которая
приводит к образованию четырёх гибридных q – электронов:
SP3
 q4 .
q4 .
Четыре равноценных q –
электрона образуют четыре равноценные σ – связи,
например, в молекуле метана CH4.
Такие молекулы (CH4,
CCl4 и т.д.) имеют пространственную конфигурацию
- тетраэдр с валентными углами 109°28'.
|
Бор, элемент третьей группы
таблицы Менделеева, имеет вапентное
окончание :
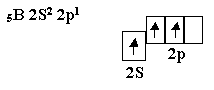 .
.
В молекуле BCl3 все три связи должны быть образованы
равноценными электродами, поэтому валентные электроны атома
бора подвергаются гибридизации. В данном случае, SP2
-гибридизации, в результате которой образуются три гибридных
q-электрона.
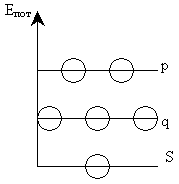 |
SP2
 q3 q3
Молекула BCl3
имеет в пространстве конфигурацию плоского треугольника
с валентными углами 120°.
|
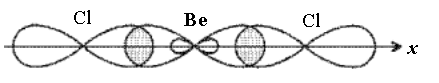
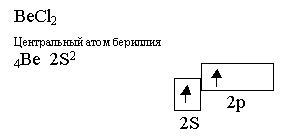
Элемент второй группы, бериллий, образует сложные частицы только
в возбуждённом состоянии:
 .
.
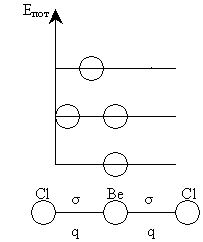 |
Валентные
электроны атома бериллия подвергаются Sp – гибридизации,
в результате которой образуется два гибридных q – электрона.
SP q2
q2
Два гибридных q – электрона,
перекрываясь, образуют две σ – связи. |
В результате образуется линейная молекула с валентным углом
180°.