1. Атомно-кристаллическое строение металлов
|
Все металлы и металлические сплавы, полученные обычными способами, представляют собой поликристаллические тела, состоящие из различно ориентированных по отношению друг к другу кристаллов. Эти кристаллы, вследствие взаимного столкновения При особых условиях металлы и сплавы могут быть получены в аморфном состоянии. Атомы в аморфных телах расположены хаотично. В дальнейшем, вместо выражения «металлы и сплавы», в тексте возможно использование термина «металлы», что соответствует принятой терминологии. Попутно отметим, что все металлы и сплавы условно подразделяют на две группы. Железо и сплавы на его основе, т. е. сталь и чугун, называют чёрными металлами, а остальные металлы и их сплавы – цветными. Атомы в кристалле, располагаясь в определённом порядке, образуют кристаллическую решётку. Эта решётка представляет собою воображаемую пространственную сетку, Расположение атомов в кристалле обычно изображают в виде пространственных так называемых элементарных кристаллических ячеек, перемещением которых можно воспроизвести пространственную кристаллическую решётку. Для металлов наиболее распространены три типа кристаллических решёток: · объёмно-центрированная кубическая (ОЦК) – атомы расположены в вершинах и центре куба. Эта решётка характерна для альфа-железа, альфа-хрома, молибдена, вольфрама, ванадия и других металлов; · гранецентрированная кубическая (ГЦК) – атомы расположены в вершинах куба · гексагональная плотноупакованная (ГПУ) – атомы расположены в углах и центре шестигранных оснований призмы, и три атома расположены в средней плоскости призмы. Эту решётку имеют магний, цинк, кадмий, альфа-цирконий и другие металлы. Расстояния между центрами ближайших атомов в элементарной ячейке называются периодами решётки. В ОЦК-рёшетке каждый атом в вершине куба одновременно принадлежит восьми элементарным ячейкам. Следовательно, на одну элементарную ячейку ОЦК-решётки приходится два атома: из них один атом находится в центре куба, а один вносят атомы, расположенные в вершинах куба. Аналогичным образом можно показать, что на одну элементарную ячейку ГЦК-решётки приходится четыре атома, а на одну ячейку ГПУ-решётки – шесть атомов.
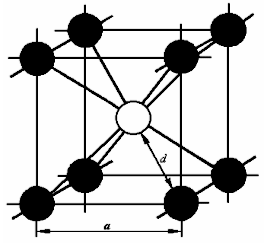
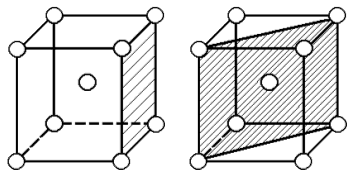
Важной характеристикой кристаллической решётки является её плотность, т. е. объём, занятый атомами. Атомы при этом рассматриваются как жёсткие шары. Плотность характеризуется координационным числом – числом атомов, находящихся на равном и наименьшем расстоянии от одного, так называемого базисного атома. На рис. 1 приведена схема кубической объёмно-центрированной решётки, где за базисный атом 0 взят атом, расположенный в центре куба. Наименьшее расстояние между атомами составляет Видно, что на равном и ближайшем расстоянии от него находится 8 атомов, расположенных в вершинах куба. Таким образом, координационное число для этой решётки 8 (обозначается К8), а коэффициент заполнения, т. е. отношение объёма, занятого атомами, к объёму ячейки, составит 68 %. Чем больше координационное число решётки, тем выше плотность упаковки атомов. Для гранецентрированной кубической и гексагональной плотноупакованной решёток координационное число 12 (принятое обозначение соответственно К12 и Г12). Эти решётки являются наиболее компактными. Коэффициент заполнения в них составляет 74 %. В специальной литературе рассматриваются такие вопросы, как кристаллографические обозначения атомных плоскостей кристаллов и индексы направлений, что необходимо, например, при объяснении такого характерного для металлических кристаллов свойства, как анизотропия – неодинаковость многих свойств – физических, химических, механических – по разным кристаллографическим направлениям. Связано это с тем, что различные плоскости заполнены атомами с различной плотностью. В качестве примера рассмотрим две плоскости в объёмно-центрированной кубической ререшётке: плоскость куба и плоскость, проходящую через элементарную ячейку (рис. 2).
Четыре атома, расположенные в вершинах квадрата, вносят Анизотропия особенно важна в технике, где используются монокристаллы. Металлы, затвердевшие в обычных условиях, состоят из множества различно ориентированных по отношению друг к другу кристаллитов. Поэтому свойства литого металла во всех направлениях более или менее одинаковы. Это явление получило название квазиизотропности, т. е. кажущейся одинаковости. |