ЛЕКЦИЯ N 4
§ 2. Спектры излучения атома водорода в теории
Бора
Изобразим на рис. 4.2. в масштабе энергетические
уровни атома водорода En в зависимости
от главного квантового числа n, в соответствии с формулой (4.10).
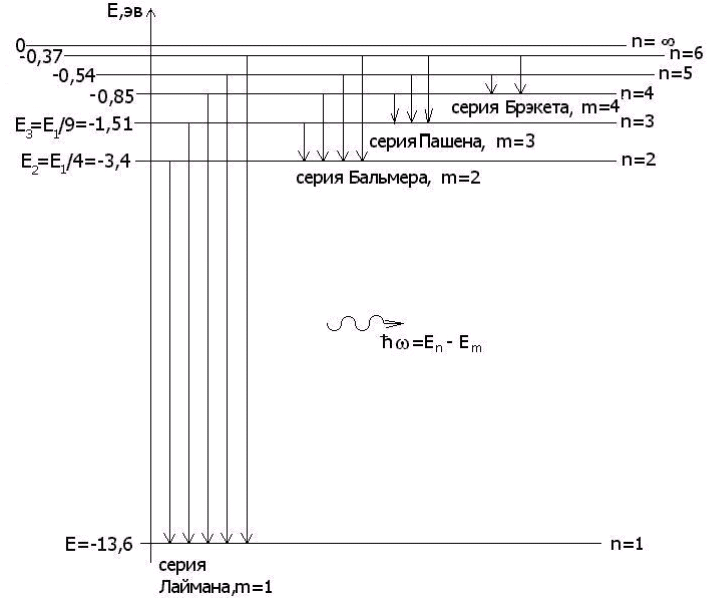
Рис. 4.2
Согласно второму постулату Бора (4.4.) энергия
излученного фотона, 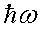 ,
равна разности энергий стационарных состояний, между которыми
происходит квантовый переход:
,
равна разности энергий стационарных состояний, между которыми
происходит квантовый переход:
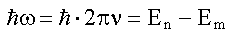 , в
случае излучения n > m.
, в
случае излучения n > m.
Подставляя сюда выражения для En
и Em, (4.8) для частоты n, получим:
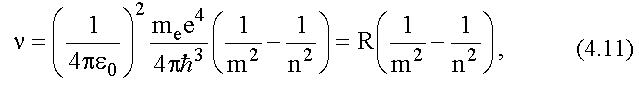
здесь
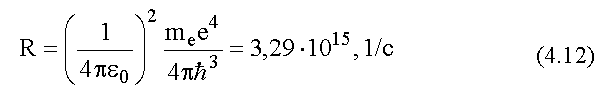
- постоянная Ридберга, она так названа в честь
шведского физика И. Ридберга.
Так как λ = c/v,
то для длины волны λ получим следующее
выражение:
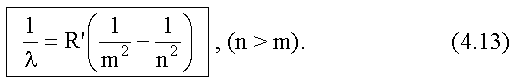
Здесь

- тоже называют постоянной Ридберга.
Из теории Бора следует, что спектр атома водорода
имеет линейчатый характер, причем, наблюдаемые линии объединены
в спектральные серии.
Задается серия номером m уровня, на который
происходит квантовый переход. Первые серии названы именами ученых-физиков:
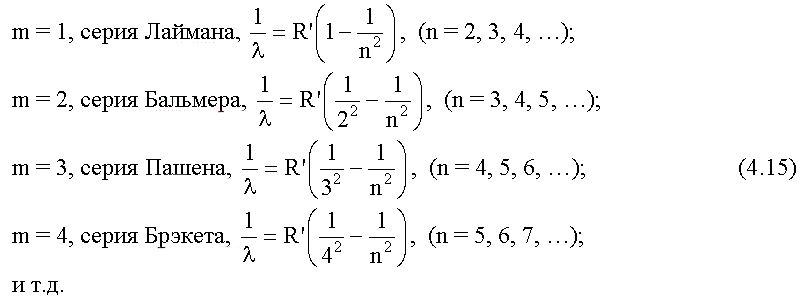
Спектры атома водорода были изучены экспериментально
до создания Бором своей теории. Хорошее совпадение экспериментальных
данных с выводами теории Бора для спектров атома водорода говорит
в пользу этой теории.
Однако, попытки применить теорию Бора к более
сложным атомам потерпели неудачу. В настоящее время теория атома
Бора представляет исторический интерес как промежуточный этап
к созданию более верной теории. Такая теория теперь существует
- это квантовая механика.
Итоги лекции N 4
-
Уравнение движения электрона в планетарной
модели атома, записанное на основе второго закона Ньютона,
позволяет атому иметь любой размер, опыт же показывает,
что размеры атомов порядка 10-10
м. Это противоречие теории и опыта получило название проблемы
размера атома.
-
Проблема стабильности атома состояла
в том, что в планетарной модели атома электрон, двигаясь по
окружности, должен, из-за наличия ускорения, непрерывно излучать
энергию и через время ~10-8
с упасть на ядро. Однако, весь наш опыт весомо свидетельствует
о стабильности атомов.
-
Проблемы эти были решены в 1913 г. Н. Бором
на основе его двух постулатов:
1) существуют стационарные состояния атом,
находясь в которых он не излучает электромагнитных волн.
Условие стационарности состояния атома - квантование момента
импульса электрона L:
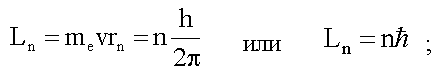
2) излучение испускается или поглощается
в виде квантов энергии 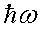 при переходе электрона из одного стационарного состояния
в другое. Энергия кванта равна разности энергий стационарных
состояний атома, между которыми происходит переход:
при переходе электрона из одного стационарного состояния
в другое. Энергия кванта равна разности энергий стационарных
состояний атома, между которыми происходит переход:
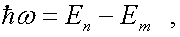
здесь Еn
- энергия стационарного состояния до перехода, Еm
- энергия стационарного состояния после перехода.
Дополнив механику Ньютона этими постулатами, Н. Бор получил
выражения для радиусов стационарных орбит rn
(см. (4.5)):
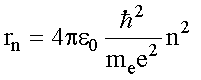
и энергии стационарных состояний атома водорода Еn
(см. (4.8)):
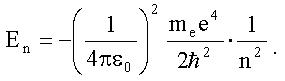
В этих формулах n - целое положительное
число: n = 1, 2, 3...
-
Из второго постулата Бора и формулы для
Еn следует выражение, определяющее
длины волн, излучаемых (и поглощаемых) атомом водорода (см.
(4.12), (4.13)):
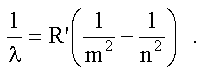
R' называют постоянной Ридберга,
ее экспериментальное значение
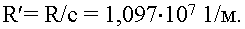
Величину R также называют
постоянной Ридбера, теория Бора дает для нее следующее выражение:
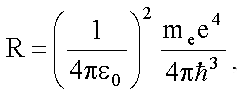
Теоретическое значение R
близко к ее экспериментальному значению.
R = 3,29 · 1015
1/c.

