 |
ФИЗИКА
|
| |
|||||
|
| |||||
 |
ФИЗИКА
|
| |
|||||
|
| |||||
ОСНОВЫ МОЛЕКУЛЯРНОЙ ФИЗИКИ И ТЕРМОДИНАМИКИ
24. Элементы термодинамики
24.4.2. Изобарический (изобарный) процесс (p = const)
Изобразим диаграмму этого процесса. В осях pV она будет прямой линией, параллельной оси V.
Работа при изобарическом процессе:
или
при p = const.
Из уравнения Клапейрона-Менделеева (22.2.4)
тогда работа для изобарического процесса следующим образом будет связана с приращением температуры:
, p = const.
Из (24.3.3.2) для произвольной массы газа имеем:
p = const.
Из (24.3.3.1):
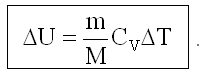
24.4.3. Изотермический процесс (T = const)
Для изотермического процесса из уравнения Клапейрона-Менделеева (22.2.4) следует, что
при T = const.
В координатах p, V диаграмма этого процесса - гипербола.
Работа при изотермическом процессе:
После интегрирования получим:
T = const.
При T = const внутренняя энергия идеального газа (24.2.1.1) не изменяется, dU = 0, значит из первого начала термодинамики (24.2.3.2) следует, что при T = const
Для конечного приращения количества тепла, с учетом полученного выше выражения для DA12 при T = const , получаем:
T = const.
24.5. Адиабатический процесс (δQ = 0)
Адиабатическим называется процесс, идущий без теплообмена с окружающей средой. Исключить теплообмен можно либо за счет хорошей теплоизоляции, либо за счет очень короткого времени протекания процесса (быстропротекающий процесс).
Выведем уравнение, описывающее адиабатический процесс.
Из первого начала термодинамики (24.2.3.2) для адиабатического процесса
имеем
Т.к.
то
Продифференцировав уравнение Клапейрона-Менделеева (22.2.4), получим:
Сложим полученное выражение с предыдущим, домноженным на R/CV, в результате получим:
В скобках стоит величина
Учтя это, получим:
или, после деления на pV:
После интегрирования имеем:
или, после простых преобразований:
Если логарифм некоторой величины равен константе, то и сама эта величина равна константе (но уже другой!). Это и есть уравнение адиабаты в окончательном виде:
Уравнение адиабаты называют также уравнением Пуассона, а величину
называют показателем адиабаты, или коэффициентом Пуассона.Напомним, что в (24.3.3.3) было получено выражение для Γ через число степеней свободы молекулы i:
24.5.1. Работа при адиабатическом процессе
После интегрирования получим:
Из полученного выражения видно, что знаки ΔA12 и ΔT при адиабатическом процессе противоположны: при адиабатическом расширении, когда ΔA12 > 0, газ охлаждается, а при адиабатическом сжатии, когда ΔA12 < 0, газ нагревается.
24.6. Энтропия. Второе начало термодинамики
Существует несколько различных формулировок второго начала термодинамики, которые эквивалентны между собой. Исторически второе начало возникло на основе анализа работы тепловых машин, и формулировки второго начала термодинамики (Клаузиуса, Кельвина, Освальда), так или иначе, связаны с принципиальными ограничениями, накладываемыми на превращение тепловой энергии (энергии хаотического, неупорядоченного движения) в механическую работу.
В современной термодинамике второе начало формулируется как закон возрастания энтропии.
Понятие энтропии можно четко и ясно сформулировать в рамках статистической термодинамики, где энтропия S определяется как величина, пропорциональная натуральному логарифму числа квантовых состояний Ω, доступных для системы:
здесь k = 1,38·10-23 Дж/К - постоянная Больцмана.
В классической механике нет аналога квантового состояния, поэтому возникает вопрос, что же именно мы должны подсчитать, как найти величину Ω - число квантовых состояний? Без некоторого привлечения понятий квантовой механики при подсчете энтропии реальных физических систем здесь принципиально нельзя обойтись.
Квантовая физика будет изложена в следующих разделах конспекта, поэтому для иллюстрации статистического определения энтропии мы воспользуемся простейшей моделью.
24.6.1. Макро- и микросостояния. Статистический вес
Макросостояние - это состояние тела, содержащее огромное число частиц (N ~ NA), заданное с помощью макроскопических величин, характеризующих все тело в целом. Такими величинами могут быть давление p, объем V, температура T, внутренняя энергия U.
Задать микросостояние - это значит задать состояния всех частиц, из которых состоит макроскопическое тело.
В классической механике состояния материальной точки (3.1.1) считается заданным, если задан ее радиус-вектор
(3.4.2) и вектор ее скорости
(3.8). Величины
и
изменяются с течением времени непрерывно, поэтому в рамках классической механики нельзя ввести понятие "число состояний, в которых может находиться частица". Такая возможность появляется при описании микрочастиц на более глубоком, квантовом уровне, где величины, характеризующие состояние микрочастиц изменяются скачкообразно, дискретно.
Статистический вес (статвес) - это число различных микросостояний, соответствующих данному макросостоянию.
Мы будем обозначать статвес греческой буквой Ω.
24.6.2. Простая модель, иллюстрирующая понятия макро-, микросостояния статистического веса
Рассмотрим идеальный газ, состоящий из N частиц, помещенных в сосуд, разделенный пополам перегородкой. В перегородке имеется небольшое отверстие, через которое молекулы могут случайным образом переходить из левой половины в правую и обратно.
Макросостояние будем задавать числом молекул N в левой половине сосуда (тогда будет известно и число молекул в правой половине N2 = N - N1). Так как давление идеального газа p = nkT, см (22.2.5), то при заданном объеме сосуда V и температуре газа T такой способ задания макросостояния определяет величину давления p в левой и правой половине сосуда, таким образом, макросостояние будет иметь определенные значения трех параметров состояния: p, V, T.
Для задания микросостояний будем считать, что частицы в чем-то отличаются друг от друга и мы их сможем пронумеровать. Тогда микросостояние будем считать заданным, если известны номера молекул, находящихся слева от перегородки (разумеется при этом известны и номера молекул, находящихся справа). Ясно, что такое задание микросостояния не является полным, но для иллюстрации нужных нам понятий это достаточно хорошая модель.
Рассмотрим простейший случай, когда число молекул N = 4. Все вторичные комбинации для этого случая представлены на следующем рисунке.
На нем в прямоугольниках, изображающих сосуд с перегородкой, цифрами обозначены номера молекул, находящихся по обе стороны перегородки. Каждый такой прямоугольник с молекулами обозначает определенное микросостояние. Прямоугольники микросостояний сгруппированы в столбики, соответствующие разным макросостояниям. Макросостояния (их у нас пять) обозначены прямоугольниками с цифрами, обозначающими число молекул слева и справа от перегородки. Всего микросостояний 16 = 24, т.к. каждая молекула, независимо от других, может находиться в двух положениях: слева и справа. Молекул 4, значит общее число микросостояний Ωобщ = 2·2·2·2 = 24 = 16. Высота столбиков микросостояний дает число различных микросостояний Ωi, соответствующих заданному макросостоянию с номером i.
Предположим, что все 16 микросостояний рассматриваемой системы равновероятны, т.е. встречаются с одинаковой частотой (это предположение носит название эргодической гипотезы). Тогда вероятность (23.2) реализации макросостояния с номером i будет пропорциональна статвесу Ωi этого состояния:
Из рассмотренного примера видно, что с наименьшей вероятностью (1/16) реализуются состояния с N1 = 0, N2 = 4 и с N1 = 4, N2 = 0, т.е. макросостояния с крайне неравномерным распределением молекул между половинками сосуда. Наибольшая вероятность у макросостояния с номером i = 3, где слева и справа от перегородки находится одинаковое число молекул.
Можно показать, что число микросостояний Ωi (N1, N-N1) нашей модельной системы для произвольного числа молекул N определяется следующим способом:
здесь
, (читается как "эн факториал"). При увеличении числа частиц растет как общее число микросостояний Ωобщ = 2N, так и увеличивается разница в статистических весах Ωi различных макросостояний. Для N = NA = 6,02·1023 г/моль вероятность того, что все молекулы соберутся в одной половине сосуда:
Это число настолько мало, что можно считать, что такое событие никогда не произойдет.
24.6.3. Равновесные и неравновесные состояния. Необратимые процессы
Макроскопическая система, состоящая из большого числа частиц (N ~ NA), согласно эргодической гипотезе проводит одинаковое время во всех своих микросостояниях. В результате с большей вероятностью реализуются макросостояния с наибольшим статистическим весом, в этих макросостояниях система проводит большую часть своего времени. Иногда система случайным образом оказывается в макросостояниях с меньшим статвесом, но так как статвес их мал, проводит в них незначительную часть своего времени. При этом физические величины, характеризующие систему, испытывают кратковременные отклонения от своих средних значений. Такие отклонения называются флуктуациями.
Равновесным называется такое макроскопическое состояние системы, которое не имеет тенденции к изменению с течением времени. Ясно, что равновесное макросостояние - это такое состояние, которое реализуется наибольшим числом микросостояний, т.е. статвес равновесного состояния максимален.
Неравновесные состояния - это состояния со статвесом меньшим, чем у равновесного. В неравновесном состоянии система находится тем меньше, чем меньше его статвес.
Необратимым называется процесс, обратный которому маловероятен.
Если собрать все молекулы в одной половине сосуда и убрать перегородку, то газ распространится на весь сосуд. Вероятность того, что он вновь соберется в одной половине сосуда, как мы подсчитали в конце раздела (24.4.2), изчезающе мала, можно считать, что такой процесс никогда не произойдет.
24.6.4. Энтропия. Формулировка второго начала термодинамики
Энтропия S определяется как натуральный логарифм статистического веса макросостояния, умноженный на постоянную Больцмана
Это выражение для энтропии получено Л. Больцманом и формула носит название формулы Больцмана.
Статистический вес Ω это и есть число доступных квантовых состояний для системы, находящейся в данном макросостоянии.
Число состояний Ω и логарифм от него - величины безразмерные, следовательно, размерность энтропии определяется размерностью постоянной Больцмана k - Дж/К.
Логарифм, как известно, функция монотонная, следовательно, свойства энтропии определяются свойствами макросостояния:
1) энтропия изолированной системы возрастает при протекании необратимого процесса (т.к. при этом возрастает статвес макросостояния);
2) энтропия системы, находящейся в равновесном состоянии, максимальна (это свойство энтропии также связано со статвесом, который максимален в равновесном состоянии).
Второе начало термодинамики утверждает, что энтропия изолированной системы не может убывать.
Второе начало термодинамики называется законом возрастания энтропии.
24.6.4.1. Связь энтропии с количеством тепла, полученным системой
Можно показать, что если система получает в обратимом процессе количество тепла δQ при температуре T, то ее энтропия возрастает на величину
Для необратимого процесса энтропия возрастает и за счет необратимости и, если система получает количество тепла δQ при температуре T, то тогда
24.6.4.2. Энтропия и беспорядок
Упорядоченным называют состояние, осуществляемое малым числом способов, т.е. у упорядоченного состояния статвес (24.6.1) мал, значит мала и энтропия (24.6.4).
Беспорядочное, или случайное, состояние - это состояние, которое может реализовываться многим числом способов.
Значит энтропия беспорядочного состояния велика.
Таким образом энтропия может служить мерой беспорядка в системе.
С ростом температуры растет энтропия системы, уменьшается ее упорядоченность.
Энтропия отдельных частей изолированной системы может уменьшаться. Но происходит это только в том случае, если в результате взаимодействия этих выделенных частей системы с ее остальными частями энтропия последних увеличивается так, что в результате энтропия всей изолированной системы возрастает. Можно сказать, что упорядоченность этих отдельных частей системы может возрасти, но только за счет увеличения беспорядка у соседей.
24.6.5. Третье начало термодинамики
При абсолютном нуле все квантовые системы переходят в основное состояние. Если оно единственное, то его статвес равен единице и энтропия
Значит, энтропия всякого тела стремится к нулю при стремлении к нулю абсолютной температуры, т.е.
Это утверждение называется третьим началом термодинамики, или теоремой Нернста.
24.6.6. Энтропия идеального газа
Для обратимого процесса
Из первого начала термодинамики (24.2.3.2), примененного к идеальному газу, следует, что:
Объединяя эти равенства, получим:
Заменим
(см. (22.2.4), уравнение Клапейрона-Менделеева).
Тогда
После интегрирования получим:
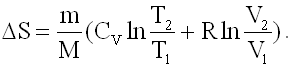
| Назад |
|
Сибирская
государственная геодезическая академия (СГГА), 2006.
|
|