2. Диаграмма состояния эвтектического типа
|
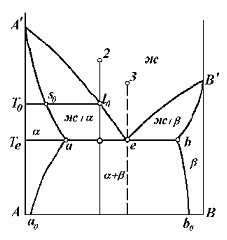
На рис. 23 приведен общий случай диаграммы состояния эвтектического типа, когда компоненты способны растворять друг друга в твёрдом состоянии до некоторого предела. Здесь линия А'еВ' – линия ликвидуса, линия А'abВ' – линия солидуса. Линия аа0 показывает изменение растворимости компонента В в А с изменением температуры, а линия bb0 – компонента А в В. Эти линии получили название линий предельной растворимости. Точки а и b характеризуют максимальную растворимость компонентов друг в друге в твёрдом состоянии, а точки а0 и b0 – предельную растворимость при комнатной температуре.
Точка e пересечения двух ветвей ликвидуса А'е и B'e называется эвтектической точкой, Поле диаграммы состоит из нескольких областей. В области ж сплавы находятся в жидком состоянии, в области ? – в состоянии твёрдого раствора компонента В в компоненте А, Видно, что фрагменты представленной на рисунке диаграммы в области составов, левее точки a0 и правее точки b0 аналогичны рассмотренной выше диаграмме с неограниченной растворимостью компонентов в твёрдом и жидком состояниях. Поэтому кристаллизация сплавов в указанных областях составов будет протекать точно так же, как и кристаллизация сплавов с полной взаимной растворимостью компонентов. После затвердевания сплавы, лежащие левее точки а0, будут состоять только из кристаллов твёрдого раствора ?, а сплавы, лежащие правее точки b0, – из кристаллов ?. На примере сплава 1 проследим за кристаллизацией сплавов, ординаты которых проходят левее точки а, но правее точки а0. Выше кривой ликвидуса сплав представляет однородную жидкость. В точке l0 на кривой ликвидуса сплав оказывается насыщенным относительно кристаллов ?-твёрдого раствора. При дальнейшем охлаждении из расплава начинают выделяться ?-кристаллы, состав которых определяется точкой s0 пересечения горизонтали, проходящей через точку l0, с кривой солидуса. С понижением температуры, вплоть до Т1, составы жидкой и твёрдой фаз будут непрерывно изменяться в соответствии с линиями ликвидуса (участок l0l1) и солидуса (участок s0s1). Количественное соотношение фаз при той или иной температуре может быть вычислено по упомянутому выше правилу отрезков. При температуре Т1 жидкость полностью затвердевает, а состав ?-кристаллов определится точкой s1. При последующем охлаждении до Т2 сплав остается однородным твёрдым раствором. В точке а1 ?-твёрдый раствор становится насыщенным компонентом В. При дальнейшем охлаждении из ?-твёрдого раствора начнут выделяться ?-кристаллы. Их состав в этот момент будет соответствовать точке b1 на кривой растворимости bb0. Процесс выделения ?-кристаллов будет продолжаться с понижением температуры, причём составы ? и ? фаз будут изменяться: ?-кристаллов – по кривой а1а0, ?-кристаллов – по кривой b1b0. Аналогично рассмотренному будет протекать кристаллизация сплавов, ордината которых проходит правее точки b, но левее точки b0. При этом с понижением температуры из ?-твёрдого раствора начнут выделяться ?-кристаллы. Составы ? и ? фаз будут изменяться согласно линиям предельной растворимости аа0 и bb0.
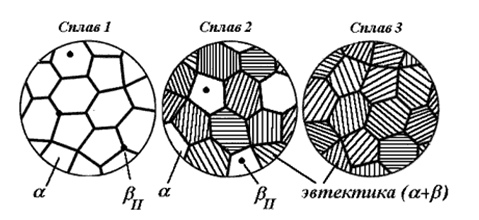
На примере сплава 2 (рис. 24) рассмотрим кристаллизацию доэвтектических сплавов, ордината которых проходит между точками a и e, т. е. пересекает эвтектическую горизонталь. При охлаждении до кривой ликвидуса (точка l0) в сплаве не происходит фазовых изменений. В интервале от Т0 до эвтектической температуры Те будет протекать двухфазное превращение ж-?-твёрдый раствор. В момент достижения температуры Те состав твёрдого раствора определится точкой a, а жидкости – точкой е. В точке е, являющейся точкой пересечения двух ветвей ликвидуса, сплав становится насыщенным как компонентом А, так и компонентом В. Следствием этого является одновременное выделение твёрдых растворов ? и ?. Так начинается трёхфазное эвтектическое превращение ж-? + ?. Составы участвующих в превращении фаз неизменны и, как уже было отмечено, определяются точками: а – для ?-твёрдого раствора, е – для жидкости, b – для ?-твёрдого раствора. Трёхфазное превращение протекает при постоянной температуре и заканчивается в тот момент, когда затвердеет вся жидкость. Теперь сплав будет состоять из двух твёрдых фаз – ? и ?, между которыми устанавливается двухфазное равновесие ?-?. При дальнейшем понижении температуры составы ? и ?-твёрдых растворов будут непрерывно изменяться вдоль кривых аа0 и bb0 соответственно. Из ?-твёрдого раствора начнут выделяться ? кристаллы, а из ?-твёрдого раствора – ?-кристаллы. Как видно, процесс будет аналогичен рассмотренному выше при охлаждении сплава 1 ниже точки а1 (см. рис. 23). Кристаллизация заэвтектических сплавов, ордината которых проходит между точками е и b, протекает аналогично кристаллизации доэвтектических сплавов, рассмотренных на примере сплава 2. Только ниже линии ликвидуса вместо ?-кристаллов выделяются В отличие от кристаллов, выпадающих непосредственно из жидкого расплава до достижения эвтектической температуры и получивших название первичных, кристаллы, выделившиеся из твёрдого раствора, называют вторичными. В рассматриваемом случае их обозначают символами ?II и ?II. Из изложенного ясно, что в эвтектическом сплаве, т. е. сплаве 3 (рис. 24), ордината которого проходит через эвтектическую точку е, затвердевание жидкости начинается непосредственно одновременным выделением из нее ? и ?-твёрдых растворов. Таким образом, сразу начинается трёхфазное превращение ж-? + ?, за которым следует двухфазное равновесие ?-?. Смесь одновременно закристаллизованных двух твёрдых растворов ? и ? называют эвтектической смесью или эвтектикой. Согласно определению эвтектика – жидкая система, находящаяся в равновесии с твёрдыми фазами, число которых равно числу компонентов системы [17]. При кристаллизации такой системы образуется механическая смесь твёрдых фаз того же состава (твёрдая эвтектика). Для уяснения особенностей распада фаз ? и ?, обусловленного понижением температуры и сопровождающегося выделением фаз ?II и ?II, подчеркнём следующее. При охлаждении доэвтектических сплавов в результате неизбежного распада имеющейся в них Вторичные кристаллы ?II и ?II, выделяющиеся из эвтектических составляющих, объединяются с соответствующими фазами эвтектики и поэтому структурно не обнаруживаются. Структуры некоторых сплавов приведены на рис. 25.
Рассматривая представленную на рис. 23 диаграмму состояния с точки зрения правила фаз, отметим следующие характерные особенности. Очевидно, что трёхфазному превращению ж-? + ?, т. е. одновременному выделению твёрдых фаз ? и ? из раствора ж, насыщенного обоими компонентами, должны предшествовать двухфазные равновесия ж-? и ж-?. Первое из равновесий описывается кривыми А'e и А'а и отвечает выделению из жидкости кристаллов ?-твёрдого раствора. Второе описывается кривыми B'e и B'b и отвечает выделению кристаллов ?-твёрдого раствора. Вариантность превращений ж-? и ж-? определяется из правила фаз согласно уравнению Габба C = 3 ? 2 = 1. Одна степень свободы указывает на то, что процесс кристаллизации как ?-твёрдого раствора, так и ?-твёрдого раствора будет протекать в интервале температур. До тех пор пока жидкость насыщена кристаллами только одного вида – ? или ?, протекает соответственно один из двухфазных процессов. Как только для составов, расположенных между точками a и b, температура понизится до эвтектической, достигается некоторое новое предельное состояние жидкости: она становится насыщенной одновременно обоими видами кристаллов. Таким образом, в равновесии оказываются три фазы постоянного состава: ?- и ?-кристаллы, составы которых соответствуют точкам a и b, и жидкость эвтектического состава. Вариантность двухкомпонентной системы, находящейся в трёх фазах, равна нулю: C = 3 ? 3 = 0. Поэтому эвтектическое превращение протекает при постоянной температуре. |